Los medicamentos huérfanos representan una esperanza vital para el diagnóstico, prevención y tratamiento de enfermedades raras. Estas condiciones, caracterizadas por su alta complejidad clínica y baja prevalencia, afectan a poblaciones reducidas, lo que plantea desafíos únicos tanto para la industria farmacéutica como para los sistemas sanitarios y salud pública.
Debido a que los estudios clínicos se realizan con poblaciones limitadas, la farmacovigilancia (la vigilancia del medicamento tras su autorización) se convierte en un pilar estratégico. Su misión es asegurar que estos tratamientos mantengan un perfil óptimo de seguridad, calidad y eficacia desde su aprobación hasta su aplicación en la vida real.
¿Qué son exactamente los medicamentos huérfanos?
Se define como medicamento huérfano a aquel fármaco destinado a enfermedades raras que, por su escasa frecuencia, carece de incentivos comerciales tradicionales para su investigación.
- El Umbral: En la Unión Europea, una patología se considera rara si afecta a menos de 5 por cada 10.000 habitantes.
- El Impacto: Existen más de 7.000 enfermedades raras identificadas. La mayoría son graves, degenerativas, de origen genético y tienen un impacto considerable en la calidad de vida del paciente.
El papel crítico de la farmacovigilancia
La farmacovigilancia es la ciencia dedicada a la detección, evaluación y prevención de eventos adversos relacionados con los medicamentos. Su objetivo central es mantener una relación beneficio-riesgo favorable durante todo el ciclo de vida del producto.
El desafío de los “Datos limitados”
A diferencia de los fármacos comunes, los medicamentos huérfanos presentan retos específicos:
- Vigilancia post-autorización estricta: Debido al bajo número de pacientes en los ensayos iniciales, ciertos efectos adversos a largo plazo solo se manifiestan tras años de uso generalizado.
- Diferenciación clínica: Es crucial distinguir entre la progresión natural de la enfermedad y un efecto secundario del medicamento.
- Notificación activa: Requiere un compromiso mayor de médicos y sanitarios para reportar cualquier anomalía.
Dato clave: La farmacovigilancia en este campo no es solo un requisito regulatorio; es la única forma de llenar los vacíos de información que dejan los ensayos clínicos pequeños y trabajar en la búsqueda de la eficacia clínica.
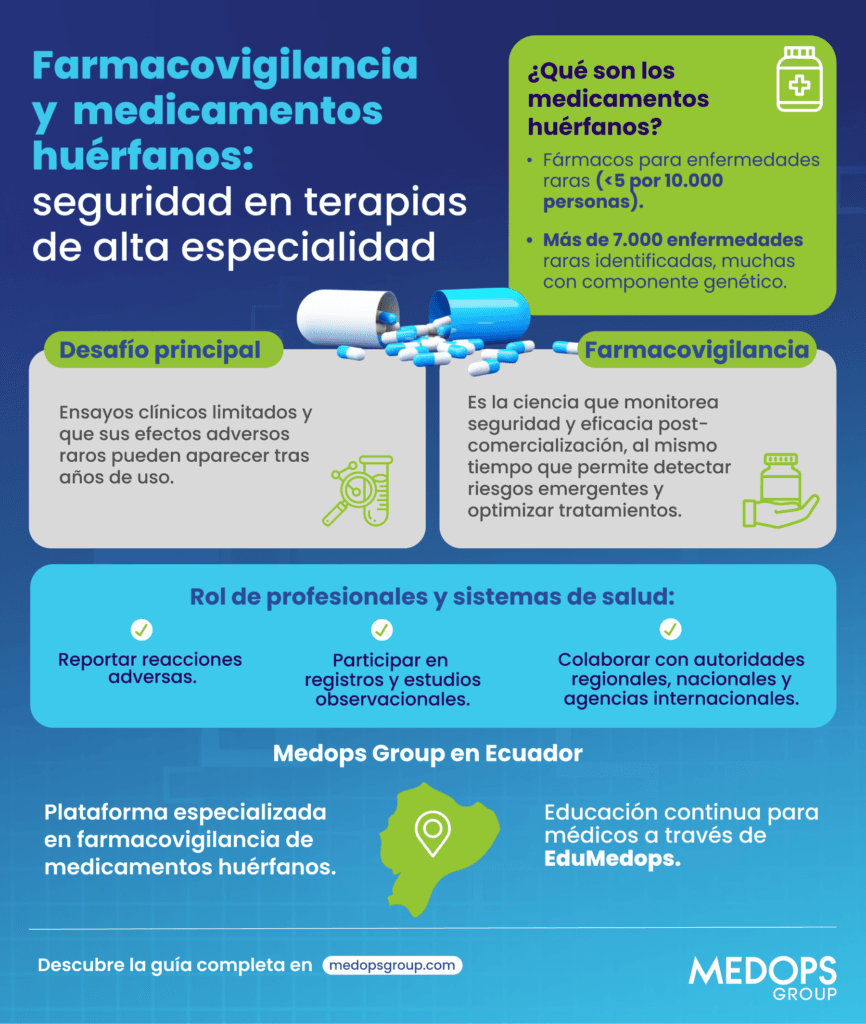
Medops Group: Liderando el acceso seguro en Ecuador
En Ecuador, la seguridad de los tratamientos para enfermedades raras depende de la sinergia entre autoridades, el Sistema Nacional de Salud, y organizaciones especializadas. Medops Group, con más de 14 años de experiencia, se ha posicionado como un referente en el acceso a tratamientos farmacológicos y nutricionales de alta especialidad.
¿Cómo marca la diferencia Medops Group?
- Plataforma especializada: Siguiendo las recomendaciones de la Organización Mundial de la Salud (OMS), Medops gestiona una plataforma de farmacovigilancia diseñada para identificar y evaluar eventos adversos en condiciones poco frecuentes.
- Cultura de reporte: Fomentan activamente que médicos y farmacéuticos reporten sospechas de reacciones, elevando el estándar de seguridad de medicamentos y terapéutica.
- Educación continua (EduMedops): A través de su iniciativa educativa, facilitan a los clínicos actualizaciones sobre avances, mecanismos de acción y seguridad, permitiendo decisiones basadas en la evidencia más reciente.
Perspectiva global: FDA, EMA y la regulación
Aunque Ecuador enfrenta sus propios desafíos regulatorios, la experiencia internacional ofrece lecciones valiosas:
- Colaboración Internacional: El intercambio de datos entre la Agencia Europea de Medicamentos (EMA) y la FDA de EE. UU. es fundamental para detectar señales de riesgo en tiempo real.
- Incentivos: Programas como la Orphan Drug Act en EE. UU. o el Reglamento (CE) 141/2000 en Europa han demostrado que ofrecer exclusividad de mercado incentiva la investigación, resultando en más terapias disponibles hoy que hace dos décadas.
Estas regulaciones subrayan la necesidad de marcos sólidos que integren la seguridad clínica desde el diseño del fármaco hasta la práctica cotidiana.
El rol indispensable del médico
Para los profesionales de la salud, la participación en farmacovigilancia es una herramienta de protección al paciente. Las estrategias clave incluyen:
- Reporte inmediato: Notificar cualquier sospecha de reacción adversa observada en consulta.
- Registros de pacientes: Participar en estudios observacionales para analizar tendencias en subgrupos y base de datos específicas.
- Colaboración con autoridades: Ayudar a mejorar la detección de señales y la respuesta rápida ante riesgos emergentes.
Un compromiso con la seguridad y la calidad
La farmacovigilancia es el garante final de la seguridad en los medicamentos huérfanos. Dado que la evidencia que arrojan algún ensayo clínico puede ser limitada por la naturaleza de las enfermedades raras, el monitoreo sistemático en la práctica real es insustituible.
Al participar activamente en la farmacovigilancia y apoyarse en aliados expertos como Medops Group, la comunidad médica no solo asegura la calidad del tratamiento, sino que promueve la equidad y el acceso seguro a terapias que transforman la vida de los pacientes.